日本QST醫院:全球首次使用重離子治療致命性室性心律失常
2023年2月,全球首例重離子治療致死性室性心律失常在日本QST醫院完成。
無痛、微創,包括準備時間在內,總治療時長不到1小時(照射時間僅8分鐘)。
以往,X射線可用于難治性室性心動過速的外照射,但存在難以完全避開治療區域周圍健康組織的問題。因此,X射線難以治療靠近供給心臟營養的冠狀動脈的病灶。日本QST醫院利用重離子線的物理特性成功避開了冠狀動脈。
迄今為止,重離子治療主要用于癌癥治療。今后,重離子治療將有望成為頑固性心律失常患者的新的治療選擇。(特殊臨床研究,日本厚生勞動省授權號jRCTs032190041,https://jrct.niph.go.jp/re)。
致命性室性心律失常,是需要緊急治療的極其嚴重的心律失常。室性心動過速是指心臟每分鐘跳動超過120次,有時會導致心室顫動,從而導致心源性猝死。可引起室性心動過速的典型器質性心臟病包括心肌梗塞、擴張型心肌病、肥厚型心肌病、致心律失常性右心室心肌病和心臟結節病。在日本,每年有60,000~80,000人死于心源性猝死,預計在老齡化社會中這一數字還會進一步增加。室性心動過速目前主要通過藥物、導管消融術和植入式心律轉復除顫器進行治療。但現實中由于多種原因,通常無法獲得所有這些治療。
體外放療有望成為室性心動過速的第四種選擇。目前,與心肌梗死或心肌病相關的室性心動過速是一個很好的指征。治療無需麻醉,照射時間極短,對患者創傷小。迄今為止,放射治療的適應癥大多局限于腫瘤疾病,但將治療應用于完全不同的疾病領域——心律失常,則極具創新性。
但這種治療方法仍在開發中,具有一定的局限性。X射線是全世界首選的放射線,但當滋養心臟的冠狀動脈與要治療的區域接近時,治療就會變得困難。因此,我們使用重離子,因為它具有能夠調節發射能量的物理特性。重離子治療為X射線高風險患者增加了新的選擇,使心律失常放射治療領域向前邁出了重要的一步。
1、臨床研究的背景
在癌癥治療中,立體定向體部放射治療(SBRT)等放射治療技術的進步使得高劑量的輻射能夠被輸送到目標,同時最大限度地減少對目標組織附近的正常器官的損害。應用該技術,自2017年以來,針對難治性致死性室性心律失常(室性心動過速)進行了外部放射治療,取得了極好的治療效果(Cuculich PS, et al. NEJM, 2017)。
日本東海大學研究小組于2019年首次在日本國內進行了這種治療,并報告了其結果(Heart Rhythm Case Rep. 2021;7:306-311.)。對于目標設定,研究者們獨立納入了使用核心臟病學的功能評估方法(99m Tc-TF、I123 MIBG、F18 FDG-PET等)以制定詳細的治療計劃(Circ Rep. 2023 5:69- 79)。 同時,研究者們一直在研究什么方法能夠更加有效地減少對健康組織的輻射暴露。
這是一個使用重離子的臨床實施方案。
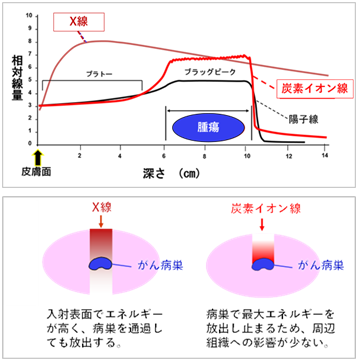
讓我們比較一下X射線和重離子束的劑量分布。如上圖所示,如果在距體表8cm深處有腫瘤,X射線進入體內時能量在靠近皮膚表面處最大,隨著它深入身體劑量逐漸減小。
而重離子束可以設置為在病灶前增大輻射能量,然后快速衰減。因此,可以集中輻射劑量并減少對正常組織的影響。此功能應用于心臟,相信將有可能減少對目標周圍微結構(冠狀動脈、主動脈瓣、房室結等)和心后器官(氣管、食道、大血管等)的影響。
2、臨床研究的實施
重離子放射治療于1994年在國立放射線科學研究所(現國立量子放射線科學技術研究所:QST醫院)開始實施,迄今已在約15,000名癌癥患者中使用。用于治療的加速器全世界有15臺,而日本就有7臺,使日本成為世界領先的重離子放射治療國家之一。
作為新一代放療手段,重離子治療一直被用于癌癥、肉瘤等惡性腫瘤疾病的治療。而這次是首次嘗試將其應用于非腫瘤疾病。患者自行進入治療室,不使用麻醉劑,治療時間含準備過程一共1小時,照射時間8分鐘。治療期間無植入式心律轉復除顫器故障或失效,生命體征平穩。治療后無急性心包炎、心力衰竭等并發癥,4天后患者安全出院。馬上就要治療1個月了,沒有任何不良反應。
放療的抗心律失常作用通常在3個月的觀察期后進行評估,但我們計劃在門診仔細監測進展情況,同時考慮到晚期放療并發癥。無論是使用X射線的SBRT,還是使用重離子,都是高精度的放療。希望未來,我們可以根據心臟靶區的位置和患者的病理特點,可以進行選擇最合適的那個治療方法。
3、未來展望
放療抑制心律失常的潛在機制正逐漸變得清晰。通過導管消融治療心律失常旨在物理中斷導致室性心動過速的異常電路。治療效果是通過高頻熱燒灼,或者通過氣體冷卻引起凍傷,使心肌組織纖維化。
據研究報導,放療從照射初期(次日~1個月)開始可觀察到心律失常抑制效果,而無需等到纖維化形成時的3~6個月。換句話說,推測早期的抗心律失常作用不一定是由纖維化引起的。
從1997年開始,本課題組就碳離子束(重離子束)作用于心臟的電生理機制進行基礎研究。在2000年的美國心臟協會科學會議上,我們首次闡明了“輻射的抗心律失常作用”。作為主要機制,我們發現碳離子束刺激心肌間隙連接蛋白連接蛋白43(Cx43)。近年來,碳離子束不僅用于室性心律失常,還用于心房顫動(Circ J. 2022)。除了在使用老齡兔的心房顫動模型中恢復連接蛋白40/43(Cx40/43) 外,推測一種機制是抑制過度的幼年交感神經。
連接蛋白在控制細胞間通訊中起著重要作用,已知它們顯著降低心臟衰竭。心臟衰竭是心律失常發展的一個因素。在衰竭的心臟中,交感神經系統和腎素-血管緊張素系統被激活以代償心臟收縮力減弱。由于交感神經系統激活可作為心律失常的調節劑,因此通常使用β受體阻滯劑來抑制它。由于重離子在改善細胞間通訊和抑制交感神經增生方面發揮作用,因此它們有可能被開發為心力衰竭的治療方法。


