日本專家談腫瘤?生物標志物
目錄
*生物標志物是什么?
*與癌癥治療相關的生物標志物有哪些?
*預估藥效的生物標志物
*評估藥物副作用的生物標志物
生物標志物是什么?
生物標志物,是指通過對人體血液,尿液等體液或組織中含有的蛋白質,基因等物質的檢測,反應疾病變化或治療效果的指標性物質。不僅可用于選擇腫瘤的治療藥物,也可用來判斷腫瘤是否存在或是否發生轉移。
通過對血液,尿液,唾液,癌細胞,癌組織等所含蛋白質,基因變化等進行測定,得到的客觀的標記物叫做生物標志物。現如今,在腫瘤的預防,診斷,治療中,經常會用到各種各樣的生物標志物,并且仍在逐漸探索中。
DNA序列便是一種生物標記物,它被稱為人體設計圖。我們可以通過DNA序列的個體差異來檢測體質。例如,是否容易罹患食管癌,與乙醛脫氫酶2(ALDH2,與酒精在人體內的分解代謝相關)的活性強弱相關。ALDH2基因有3種類型,根據飲酒后面部顏色變化,在某種程度上可以判斷出是哪種類型,也可通過對唾液的基因檢測判斷出來。
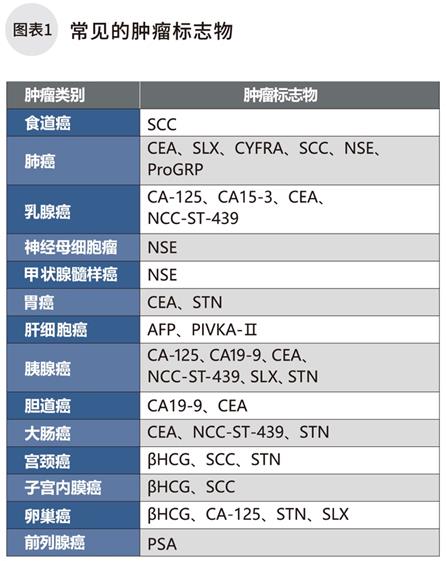
血液檢查測定的腫瘤標志物也是生物標志物的一種(圖表1)。
腫瘤標志物的測定,通常用于常規體檢中的癌癥早期篩查,也是診斷癌癥是否復發/轉移的檢查項目之一。
但遺憾的是,現階段尚不能通過測定腫瘤標志物就實現腫瘤的預防和早期發現。
癌癥治療中,為了精準地選擇治療藥物,需要測定各種生物標志物。主要是通過活檢或手術的方式采取腫瘤組織進行分析和檢測。
★腫瘤標志物是什么?
腫瘤標志物是癌細胞在增殖過程中釋放到血液或體液中的特殊物質。通常觀測藥物治療或放療后的腫瘤標志物的數值變化,來提示腫瘤是否復發。例如,在血液檢查中,可能會測定圖表1中的腫瘤標志物。但是,數值上升并非一定就是腫瘤,而數值未上升也并非就等于沒有腫瘤。單憑腫瘤標志物的數值不能用來診斷腫瘤,是否進展/消退/復發,只能作為診斷時的參考數據。
★癌癥的發生和癌細胞增殖的機制
癌細胞,是由正常細胞中的基因發生持續性突變后形成的。癌細胞會形成異常組織,在基因突變進一步累積后,增殖速度急速上升,最終失控而無限制增殖。
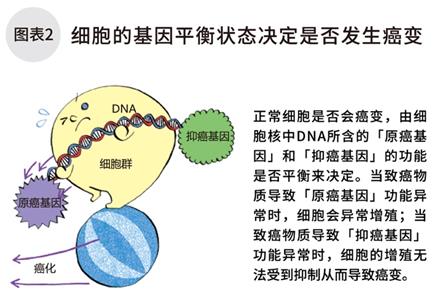
即使我們的身體出現異常細胞,具有“剎車”功能的「抑癌基因」會隨即啟動,阻止異常細胞的增殖,并將其修復成正常細胞。但如果促進細胞增殖的「原癌基因」發生異常,增殖狀態便像踩了油門一樣,一發不可收拾。此時,如果「抑癌基因」受損傷,便無法啟動剎車功能,異常細胞便會持續增殖。(圖表2)
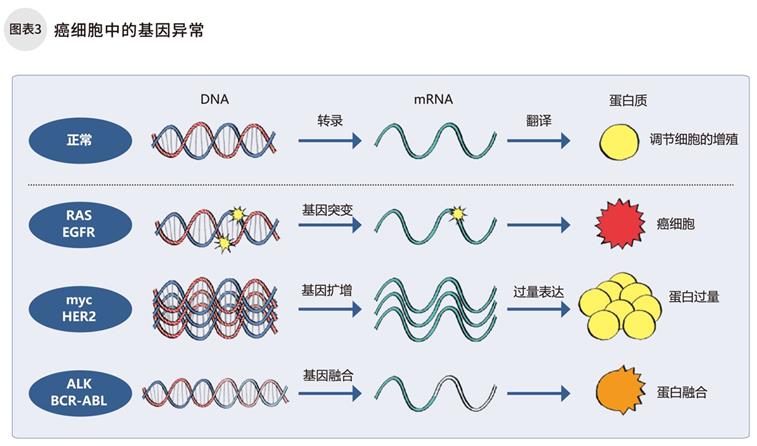
長期吸煙,暴露在霉菌等各種致癌物質的環境中,是導致基因突變的原因之一。突變的基因產生異常蛋白質,促使了細胞無限制增殖。原本分開的2個基因在融合后,也可能生成異常蛋白,導致細胞失控無限制增殖。(圖表3)。另外,即使基因沒有突變,DNA也會因細胞分裂發生持續變異,導致癌變。
隨著癌細胞增殖原因的逐漸明確,以癌癥相關基因和蛋白為靶點的靶向治療藥物被不斷開發出來。
與癌癥治療相關的生物標志物有哪些?
在現階段的癌癥治療中,生物標志物主要用來針對特定的藥物療法,預測其療效,副作用及預后。
★預測藥物的療效
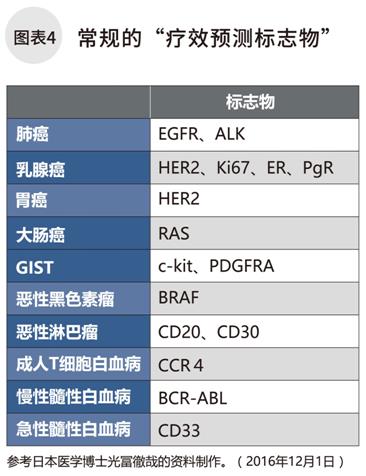
癌癥的治療主要有手術治療,放療,藥物治療,免疫治療4種方式。目前癌癥治療中常用的生物標志物主要用來選擇藥物治療方案,預測療效。我們稱之為“療效預測標志物”。
療效預測標志物(圖表4),有肺癌的EGFR基因突變,ALK基因融合,乳腺癌或胃癌的HER2基因過表達等。這些標志物本身就是參與癌細胞增殖的因子。當這些基因發生突變,出現蛋白異常表達時,癌細胞增殖的開關就會打開,無限制地增殖下去。
以癌細胞增殖相關因子(蛋白質或基因)為靶點的“靶向藥物”是新型的癌癥治療藥物。相關生物標志物的測定也伴隨著靶向藥物的出現在進步。例如,EGFR基因突變的測定,就是用來預測EGFR抑制劑療效的。乳腺癌的雌激素受體(ER)和孕激素受體(PgR)的測定是用來預測內分泌療法的治療效果的。
通常在診斷癌癥,做病理檢測時測定生物標志物。檢測樣本可以通過穿刺活檢獲取。也可使用手術切除的組織標本。白血病的話,要在髂骨或胸骨上進行骨髓穿刺,抽出骨髓液樣本進行測定,分析是否出現基因突變或特異蛋白。
治療藥物失效,或腫瘤發生進展,復發時也會進行相應的標志物檢測。
★療效預測標志物與個性化治療
療效預測標志物,可以預測患者是否能從某種治療中獲益,從而幫助患者在選擇最合適,療效最好的治療方案。
但也難免會發生在測定標志物后,接受了某種特定藥物的治療并沒有療效的情況。例如,針對大腸癌患者進行的PAS(KRAS or NRAS)基因檢測中發現了基因突變,選擇了EGFR單抗藥物的治療,但是結果顯示并無療效。
癌癥的治療藥物會產生各種副作用,其中不乏攸關性命的嚴重副作用。因此,盡可能避免使用無效藥物,以及藥物帶來的副作用,可以提高患者的生活質量。
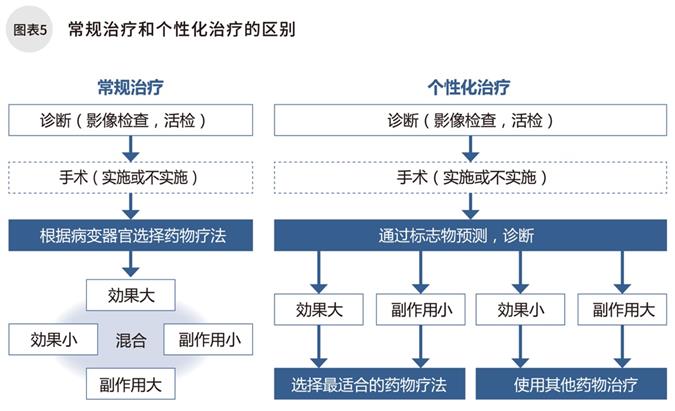
以往的藥物療法中,對于不同的患病器官,治療方式是基本相同的。但是近年來,通過測定標志物,結合腫瘤的類別和患者的自身情況,選擇最有效的藥物治療,即“個性化治療”越來越收到重視。(圖表5)
★ 預后預測標志物與副作用預測標志物
標志物中還有一類用來預測預后。比如,測定乳腺癌復發風險的oncotype DX和MammaPrint就是預后預測標志物。如果雌激素受體(ER)呈陽性,通常腫瘤進展比較緩慢,屬于穩定型;如果HER2過表達,則需要使用HER2抗體藥物來治療,改善預后。像ER、HER2這類用來預測特定藥物療效的標志物,同時也是用來預測預后的標志物。
副作用預測標志物,是通過檢測患者體內是否含有降解某種化療藥物毒性的酶,來提示副作用的嚴重程度,從而避免發生嚴重副作用。通常在使用某種化療藥物前,通過血液檢測。
★伴隨診斷是什么?
診斷癌癥,檢測各種標志物時你可能會聽到過一個詞語--“伴隨診斷”。伴隨診斷,是針對期待某種治療藥物藥效的患者,或者強烈恐懼副作用的患者,使用手術/活檢采取的腫瘤組織進行的體外診斷,而不是直接給患者配藥或配備裝備。最近,靶向藥物等新型藥物的開發,也帶動了伴隨診斷的需求大大增加。
有關預估藥效的標志物
預估藥物療法的療效時,肺癌采用EGFR基因檢測,ALK融合基因檢測;乳腺癌或胃癌采用HER2基因擴增/蛋白過表達的檢測;大腸癌采用RAS基因檢測。根據腫瘤的性質選擇最合適的藥物療法,非常重要。
預估藥物療法的療效時,結合每位患者的腫瘤類型,測定相應的標志物,能夠幫助患者選擇受益最大的治療藥物。根據腫瘤的類別不同,標志物的有效性也不同。
《肺癌》
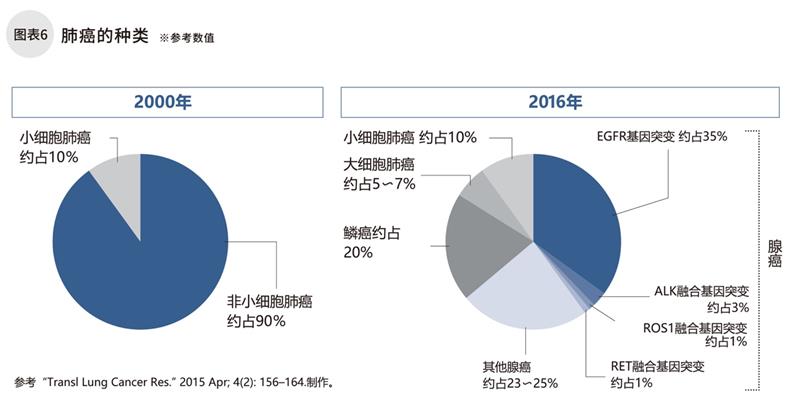
本世紀初,肺癌的藥物療法只針對非小細胞肺癌和小細胞肺癌兩類。現在,非小細胞肺癌中的腺癌根據致病基因有了更加細致的分類(圖表6)。其中,EGFR基因突變導致的肺腺癌在日本占有很大的比例。
EGFR基因檢測,作為預估藥效的標志物,是針對非小細胞癌中有必要接受藥物療法的患者實施的。可以通過診斷時氣管鏡下活檢或手術切除的部分腫瘤組織來檢測。
EGFR是分布于癌細胞表面的蛋白,向細胞內部傳遞細胞增殖的必要信號。EGFR一旦發生突變,就像打開了開關,癌細胞就會無限制的增殖下去。
如果檢測到EGFR基因突變,一線治療方案是使用療效最好的EGFR抑制劑。它可以阻斷EGFR的異常活化,抑制癌細胞的增殖。一線藥物有吉非替尼,埃羅替尼,二線藥物有阿法替尼。
治療的過程中,這些藥物可能會逐漸失效,導致癌細胞繼續增殖。此時需要再次進行腫瘤組織活檢,進行另外一個標志物EGFRT790M的檢測。T790M突變的話,可使用三線EGFR抑制劑--奧希替尼。
ALK 融合基因,是ALK基因和EML4基因融合產生的異常基因。該基因合成的ALK融蛋白會激活其他相關蛋白,促使癌細胞無限制的增殖。具有ALK融合基因的患者占肺腺癌患者的3%左右。
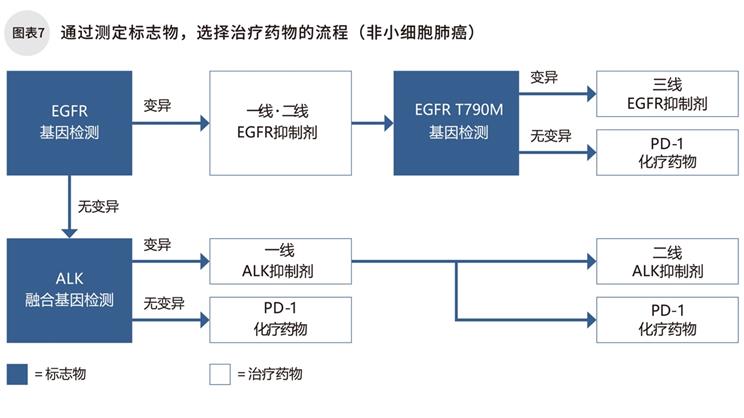
ALK 融合基因呈陽性的話,可以使用ALK抑制劑來抑制ALK融合基因的表達,阻止癌細胞的增殖(圖表7)。
EGFR基因突變和ALK融合基因兩者均為陰性,可考慮使用免疫檢查點抑制劑PD-1來阻斷免疫抑制;如果兩者均為陽性,而EGFR抑制劑和ALK抑制劑都失效時,也可以考慮使用PD-1。對與非小細胞肺癌中肺鱗癌的患者,不需要做EGFR基因檢測和ALK融合基因檢測,可以直接使用PD-1。
在使用免疫檢查點抑制劑時,可以檢測癌細胞表面具有免疫抑制功能的PD-L1蛋白表達,用來預測藥效。
針對非小細胞肺癌,ROS1融合基因陽性的治療藥物正在研制開發。
《乳腺癌》
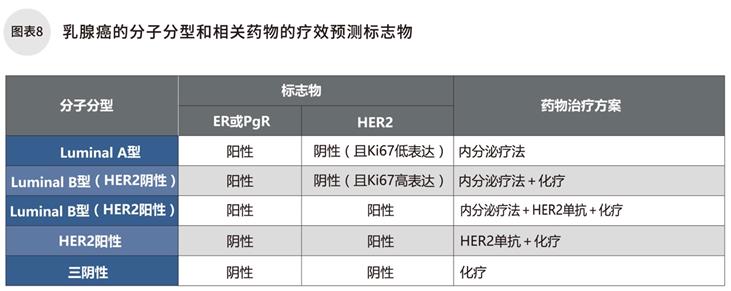
除了局限于乳腺導管的非浸潤癌以外,大多數乳腺癌患者都是通過檢測療效預測標志物,來選擇藥物療法的。主要的標志物:雌激素受體(ER),孕激素受體(PgR)及HER2過表達。根據這幾種標志物的檢測結果,以及Ki67(反應細胞增殖能力)的數值,來進行分子分型,選擇最適合的藥物治療方案。(圖表8)
療效預測標志物,通過腫瘤診斷時活檢采取的細胞或組織進行檢測。乳腺癌的細胞中如果存在激素受體,說明癌細胞在奪取雌激素,并且在增殖。ER陽性或PgR陽性時,可以進行內分泌治療,阻止癌細胞奪取雌激素,抑制癌細胞生長。絕經前患者可使用雌激素類藥物和抑制卵巢功能的LH-RH受體拮抗劑;絕經后患者可使用芳香化酶抑制劑或雌激素類藥物。內分泌療法是否需要附加化療,由Ki67決定。Ki67高表達時,可進行內分泌療法聯合化療。也可通過檢測oncotype DX或MammaPrint來預測復發風險,判斷是否有必要進行化療。
HER2是存在于細胞表皮上的蛋白。過高表達(HER2陽性)則表示癌細胞在持續增殖。可使用HER2抗體藥物聯合化療的藥物療法。
乳腺癌復發時,可再次通過活檢,檢測激素受體,HER2等標志物來選擇最適合的藥物療法。
《胃癌》
胃癌與乳腺癌相同,也有可能是因為HER2的過表達導致癌細胞的增殖。無法手術的晚期胃癌,復發/轉移時有必要測定HER2基因和蛋白的表達狀態。需要通過內視鏡取活檢或手術切除的腫瘤組織進行測定。
HER2陽性,可以選擇HER2單抗聯合化療為一線治療方案。HER2陰性或HER2單抗失效時,可遵循以往的常規化療。
《大腸癌》
無法手術的晚期大腸癌,或大腸癌復發時,通過標志物RAS基因檢測,選擇最適合的藥物療法。通過內視鏡或手術采取癌組織,進行KRAS和NRAS基因檢測確認是否發生突變。
KRAS和NRAS基因,無論哪一個突變,EGFR單抗藥物都會無效。兩者中只要有一個屬于無變異的“野生型”基因,患者身體狀況良好的話,都可以考慮EGFR單抗聯合多藥物化療作為首選治療方案。
《GIST (胃腸道間質瘤)》
GIST (胃腸道質腫瘤),是發生在胃,小腸,大腸等消化道肌層的惡性腫瘤。患者中約80~90%的人細胞中存在c-kit基因突變導致的KIT蛋白異常。剩下的患者大多數竄在PDGFRA基因突變導致。
GIST的標志物c-kit基因需要通過內視鏡等采取病變組織進行檢測。該檢測對于BCR-ABL激酶抑制劑的藥效預測和腫瘤惡性程度的判斷發揮重要作用。c-kit陰性時,還需要檢測PDGFRA基因是否突變導致。
在GIST的治療中,無法手術/發生其他器官轉移/術后復發機率高,這幾種情況都可以進行藥物治療。c-kit陽性或PDGFRA陽性,在接受藥物療法時,可以考慮使用BCR-ABL激酶抑制劑--伊馬替尼。
BCR-ABL激酶抑制劑可以抑制KIT過表達,而KIT蛋白會促進癌細胞的增殖。伊馬替尼失效時可以考慮使用酪氨酸激酶抑制劑--舒尼替尼。這些藥物都失效后,可以考慮使用多激酶抑制劑-瑞格菲尼。
《惡性黑色素瘤》
BRAF基因突變,是針對手術無法切除,或已發生其他器官轉移的惡性黑色素瘤患者,在選擇最有效藥物治療時使用的療效預測標志物。腫瘤組織如果存在RAF突變,可優先選擇BRAF抑制劑作為一線治療方案。BRAF無突變,可考慮使用免疫檢查點抑制劑藥物PD-1或CTLA-4。
《惡性淋巴瘤》
惡性淋巴瘤的治療中,一般采用以細胞表面特異性蛋白為靶點的抗體藥物。通過對診斷時手術切除的淋巴結進行活檢來確定淋巴瘤的性質。同時通過免疫組化檢測特異性蛋白。
對于B細胞性非霍奇金淋巴瘤,可檢查細胞表面是否存在“CD20抗原”蛋白。CD20陽性,可單獨使用CD20單抗藥物,或聯合多藥劑化療進行藥物治療。
CD20陽性患者發生復發,或藥物治療無效時,可以聯合放射線同位素,以CD20為靶點放療來攻擊淋巴瘤。
霍奇金淋巴瘤,未分化的大細胞淋巴瘤復發時,如果發現CD30抗原蛋白,可以考慮使用CD30抗體藥物。聯合化療藥物,以CD30為靶點攻擊淋巴瘤。
《成人T細胞白血病淋巴瘤(ATL) 》
ATL治療中如果出現CCR4表達陽性,可使用CCR4抗體藥物。以CCR4為靶點攻擊癌細胞。約90%的ALT患者為CCR4陽性。
末梢性T細胞淋巴瘤,皮膚T細胞淋巴瘤復發時如果發現CCR4陽性,也可使用CCR4抗體藥物。
《慢性骨髓性白血病(CML)》
診斷CML時,需要在患者髂骨處穿刺取骨髓液進行檢測。如果確診為CML,可以使用GIST治療中常用的BCR-ABL抑制劑,抑制BCR-ABL的異常表達,阻止其發出細胞增殖的指令,從而緩解病情。BCR-ABL基因檢測不僅能夠確診CML,還可以預測BCR-ABL抑制劑的療效。
服用BCR-ABL抑制劑后,有些患者的癌細胞會消失。但是長時間服用可能出現耐藥。此時,可以更換其他BCR-ABL抑制劑。但是需要再次進行骨髓穿刺,進行T315I基因檢測。如T315I基因突變,可考慮服用普納替尼。
《 急性骨髓性白血病(AML)》
AML如出現CD33抗原表達,在復發時可使用CD33抗體藥物。其他以致癌基因或蛋白為靶點的藥物也在積極開發中。
《 根據致癌基因,實施個性化治療 》
上述這些通過測定標志物確定致癌基因,選擇最適合藥物的個性化治療已經在廣泛開展。在乳腺癌或胃癌中,HER2基因擴增和蛋白過表達說明:致癌基因和癌變器官無關。另外免疫檢查點抑制劑對許多癌癥都有效果。以往都是根據病變部位的器官分類來選擇藥物療法的。今后,根據致癌基因選擇最適合藥物療法的時代即將到來。
《 療效預測標志物與藥物副作用 》
療效預測標志物,終究是用來預測療效的,并不能預測副作用的強度。即使根據標志物選擇的藥物,也可能會出現強烈的副作用。因此,患者需要和主治醫生或其他醫療人員保持溝通,在充分理解各種治療方案的療效和可能出現的副作用后,謹慎做出選擇。同時患者還需注意提前確認何種情況下必須聯系醫院,以及醫院的緊急聯系方式。
有關評估藥物副作用的標志物
通過血液檢查分析DNA序列,可以檢測出是否為容易出現副作用的體質。
現階段的癌癥治療中常用的預測副作用的標志物是UGT1A1基因。這是預測DNA拓撲異構酶抑制劑--伊立替康副作用的標記物。伊立替康是肺癌,胃癌,乳腺癌,大腸癌,宮頸癌,卵巢癌,胰腺癌,惡性淋巴瘤等藥物療法中常用的化療藥物。可能引起骨髓抑制(白細胞/血小板/中性粒細胞減少),腹瀉等嚴重的副作用。
UGT1A1基因在服用伊立替康前通過血液檢查來測定,可以通過分析DNA序列的個體差異,判斷患者是否為易出現中性粒細胞減少副作用的體質。中性粒細胞在修復免疫和傷口時非常重要,大幅度的數量減少會導致死亡。
檢測中被確定為高風險的患者,遺傳了父母雙方肝臟解毒能力差的體質。有關這種解讀能力的遺傳多樣性有兩種類型,只要從父母中的一方遺傳了這兩種類型,就是高危型。同等劑量的藥物在高危患者的肝臟中停留時間較長,容易引起嚴重的中性粒細胞減少。在以日本人為對象的研究中,高危患者約占10%,中性粒細胞減少的發生率約在80~100%.因此高危患者需要考慮減少伊立替康的劑量。
但是,該檢測在伊立替康用藥時不是必須的檢查項目,根據醫院不同,規定不同。另外,該檢測是有局限性的。非高危患者也可能會出現嚴重的中性粒細胞減少癥狀。但使用伊立替康容易導致副作用,并不代表其他的化療藥物也會出現嚴重副作用。
除了UGT1A1基因外,在日本,尚無證據表明有其他更有效的副作用預測標志物。


